Die Diagnose eines Gehirntumors ist eine komplexe Erkrankung des zentralen Nervensystems, die durch abnormales Zellwachstum gekennzeichnet ist. Für Betroffene und ihre Angehörigen bedeutet dies oft den Einstieg in eine Welt voller medizinischer Fachbegriffe. Was genau bedeuten diese Begriffe? Wie wird ein Tumor eingestuft? Und welche Behandlungsoptionen gibt es heute? Die Antwort liegt nicht nur in der Biopsie unter dem Mikroskop, sondern zunehmend in der molekularen Genetik. Dieser Artikel klärt über die aktuellen Standards auf - basierend auf der neuesten WHO-Klassifikation (WHO CNS5) von 2021 - und erklärt, wie moderne Therapien funktionieren.
Die neue Ära der Klassifikation: WHO CNS5
Jahrzehntelang haben Ärzte sich primär auf das Aussehen der Zellen verlassen, um einen Gehirntumor zu bewerten. Das änderte sich grundlegend mit der fünften Ausgabe der WHO-Klassifikation der Tumoren des Zentralnervensystems, auch bekannt als WHO CNS5. Diese Ausgabe, veröffentlicht im Jahr 2021, markiert einen Paradigmenwechsel. Statt nur zu schauen, wie chaotisch die Zellen aussehen (Histologie), integrieren Pathologen nun zwingend molekular-genetische Marker.
Warum ist das wichtig? Weil zwei Tumoren, die unter dem Mikroskop identisch aussehen, biologisch völlig unterschiedlich sein können. Ein Beispiel: Ein Glioblastom, das den IDH-Mutationstatus "wildtyp" hat, verhält sich aggressiv. Ein ähnlicher Tumor mit einer IDH-Mutation kann langsamer wachsen und besser auf Behandlungen ansprechen. Dr. David Schiff von der University of Virginia fasste es treffend zusammen: Die Integration dieser Marker hat die diagnostische Genauigkeit im Vergleich zur reinen Histologie um 35-40 % verbessert. Das bedeutet für Sie: Die Diagnose ist präziser, und damit auch die Prognose und Therapieplanung.
Verständlich erklärt: Die WHO-Grade 1 bis 4
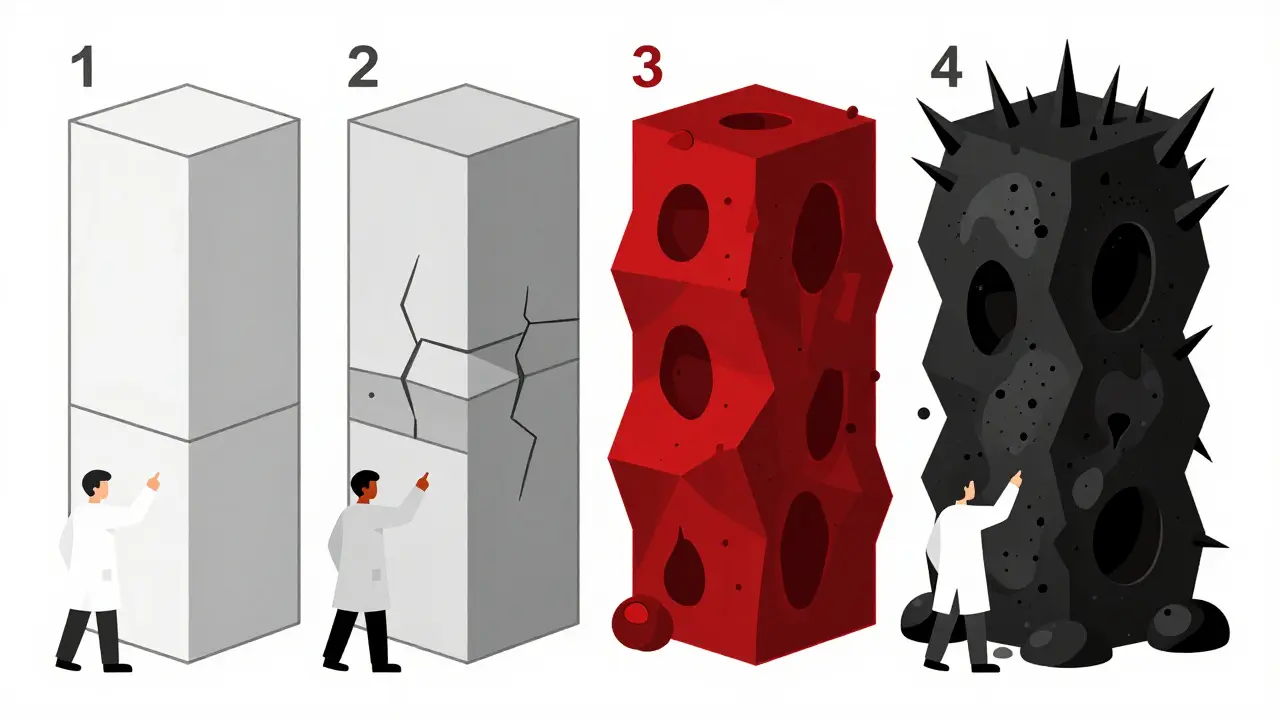
Der Begriff "Grad" oder "Stufe" beschreibt das Wachstumsverhalten des Tumors. Es handelt sich dabei um eine Skala von 1 bis 4. Wichtig zu verstehen: Der Grad sagt nichts über die Größe des Tumors aus, sondern darüber, wie schnell er wächst und wie wahrscheinlich er wiederkehrt.
- Grad 1 (Niedriggradig): Die Zellen sehen fast normal aus. Der Tumor wächst sehr langsam und hat meist klare Grenzen. Oft kann er vollständig entfernt werden. Beispiele sind pilozytäre Astrozytome.
- Grad 2 (Niedriggradig): Die Zellen zeigen erste Abnormalitäten. Diese Tumoren infiltrieren das gesunde Hirngewebe, was eine vollständige Entfernung schwierig macht. Sie können sich im Laufe der Zeit in höhere Grade verwandeln.
- Grad 3 (Hochgradig): Hier sprechen wir von malignen Tumoren. Die Zellen vermehren sich aktiv und invasiv. Diese Tumoren neigen dazu, zurückzukehren und benötigen intensive Therapien.
- Grad 4 (Hochgradig): Das sind die aggressivsten Formen. Sie wachsen rasant, bilden eigene Blutgefäße und weisen oft Nekrosen (abgestorbenes Gewebe) auf. Das Glioblastom ist hier der häufigste Vertreter bei Erwachsenen.
Eine wichtige Neuerung in der WHO CNS5 ist die sogenannte "innerhalb-des-Tumor-Typs"-Einstufung. Nicht jeder Tumor kann jeden Grad erreichen. Zum Beispiel gibt es Meningeome nur in den Graden 1 bis 3. Oligodengogliome liegen typischerweise zwischen Grad 2 und 3. Das hilft Ärzten, realistische Erwartungen zu setzen.
| WHO-Grad | Wachstumsgeschwindigkeit | Invasivität | Typische Beispiele |
|---|---|---|---|
| 1 | Sehr langsam | Niedrig (klare Ränder) | Pilozytäres Astrozytom, Meningiom (Grad 1) |
| 2 | Langsam bis moderat | Mittel (infiltrativ) | d>Astrozytom IDH-mutant, Oligodendrogliom |
| 3 | Schnell | Hoch (aggressiv) | Anaplastisches Astrozytom, Oligodendrogliom |
| 4 | Sehr schnell | Sehr hoch (nekrotisch) | Glioblastom, H3-gliomas |
Die wichtigsten Tumorarten im Detail
Nicht alle Gehirntumore sind gleich. Die Herkunft der Zellen bestimmt die Art des Tumors. Hier sind die häufigsten Kategorien:
Gliome
Gliome entstehen aus den Stützzellen des Gehirns (Gliazellen). Sie machen den Großteil der primären bösartigen Hirntumore aus.
- Astrozytome: Können alle Grade (1-4) abdecken. Entscheidend ist der IDH-Status. IDH-mutante Astrozytome haben eine bessere Prognose als IDH-wildtyp-Tumoren.
- Oligodendrogliome: Treten meist in den Graden 2 und 3 auf. Sie sind durch eine spezifische genetische Veränderung (1p/19q Codeletion) gekennzeichnet und sprechen oft gut auf Chemotherapie an.
- Glioblastom (GBM): Der aggressivste Gliom-Typ (immer Grad 4, IDH-wildtyp). Er betrifft vorwiegend ältere Erwachsene und wächst extrem schnell.
Meningeome
Diese Tumore entstehen aus den Hirnhäuten (Meningen), nicht aus dem Gehirn selbst. Die meisten Meningeome sind gutartig (Grad 1) und lassen sich operativ entfernen. Nur ein kleiner Prozentsatz ist bösartig (Grad 3).
Kraniopharyngeom
Häufig bei Kindern und Jugendlichen gefunden, liegen sie nahe der Hypophyse. Obwohl sie oft histologisch niedriggradig sind, können sie aufgrund ihrer Lage schwer zu behandeln sein.
Multimodale Therapien: Mehr als nur Operation
Die Behandlung von Gehirntumoren ist heute ein Teamwork aus Neurochirurgen, Strahlentherapeuten, Onkologen und Neuropathologen. Man spricht von einer multimodalen Therapie.
- Neurochirurgie: Das Ziel ist die maximale sichere Resektion. Je mehr Tumorgewebe entfernt werden kann, desto besser ist die Prognose. Moderne Techniken wie neuronavigationssysteme und intraoperative MRTs helfen, das gesunde Hirngewebe zu schonen.
- Strahlentherapie: Nach der Operation folgt oft eine Bestrahlung, um verbliebene Zellen zu bekämpfen. Bei Glioblastomen ist dies Standard.
- Chemotherapie: Medikamente wie Temozolomid werden häufig eingesetzt. Besonders relevant ist hier der MGMT-Promotor-Status. Ist der Promotor methyliert, spricht der Tumor besser auf Temozolomid an.
- Zielgerichtete Therapien: Ein Durchbruch war die Zulassung von Vorasidenib (2023) für IDH-mutante Gliome Grad 2. Diese Tablette hemmt direkt den fehlerhaften Enzymweg in den Tumorzellen und hat in Studien die progressionsfreie Überlebenszeit signifikant verlängert.
Diagnostik und Kosten: Was Patienten wissen sollten
Die Wegstrecke von der ersten Symptomatik bis zur finalen Diagnose kann frustrierend sein. Eine Studie der Brain Tumour Charity zeigte, dass 68 % der Patienten Wartezeiten von über 8 Wochen erlebten. Die molekulare Diagnostik ist zwar teuer - laut Johns Hopkins kommen je nach Testpaket 3.200 bis 5.800 Dollar hinzu -, aber sie ist unverzichtbar für die richtige Therapieauswahl.
Ein weiterer Fortschritt ist die Verkürzung der Wartezeiten für Ergebnisse. Dank neuer Antikörper-Tests (wie Ventana IDH1 R132H) konnte die FDA die Zeit für molekulare Tests von bis zu drei Wochen auf etwa 48 Stunden reduzieren. Das beschleunigt den Behandlungsstart erheblich.
Ausblick: Liquid Biopsy und Personalisierte Medizin
Die Zukunft gehört der minimal-invasiven Diagnostik. Forscher arbeiten an "Liquid Biopsies", bei denen tumor-spezifische DNA aus der Liquorflüssigkeit (Rückenmarksflüssigkeit) analysiert wird. Erste Studien zeigten eine Sensitivität von 89 %. Das könnte in Zukunft wiederholte Biopsien überflüssig machen, um das Ansprechen auf die Therapie zu kontrollieren.
Was bedeutet der IDH-Status bei einem Gehirntumor?
IDH steht für Isocitrat-Dehydrogenase. Eine Mutation in diesem Gen (IDH-mutant) ist ein günstiger prognostischer Faktor bei vielen Gliomen. Es bedeutet, dass der Tumor tendenziell langsamer wächst und besser auf Therapien anspricht als IDH-wildtyp-Tumoren. Seit der WHO-Klassifikation 2021 ist dieser Status zwingend für die Diagnose erforderlich.
Wie lange dauert die Diagnosestellung bei Verdacht auf Gehirntumor?
Von der Biopsie bis zur finalen molekularen Diagnose vergehen typischerweise 7 bis 10 Werktage. Allerdings können Wartezeiten für die Erstuntersuchungen (MRT, Neurologie) länger sein. Studien berichten durchschnittlich von 8 bis 14 Wochen Verzögerung, abhängig vom Gesundheitssystem und der Dringlichkeit.
Ist ein Gehirntumor immer Krebs?
Nein. Tumore der Grade 1 und 2 werden als niedriggradig eingestuft und sind oft gutartig oder haben ein sehr geringes Metastasenrisiko. Sie können jedoch lokal Druck auf das Hirn ausüben. Hochgradige Tumore (Grad 3 und 4) sind malign, also krebsartig, und neigen zum raschen Wachstum und zur Rückkehr.
Was ist die Rolle der Strahlentherapie?
Die Strahlentherapie nutzt ionisierende Strahlung, um das Wachstum von Tumorzellen zu stoppen oder sie abzutöten. Sie wird meist nach der Operation eingesetzt, um verbliebene Mikroreste zu bekämpfen. Bei aggressiven Tumoren wie dem Glioblastom ist sie Teil des Standardprotokolls (Stupp-Protokoll).
Welche neuen Medikamente gibt es 2026?
Ein wichtiger Meilenstein war die Zulassung von Vorasidenib für IDH-mutante Gliome Grad 2. Zudem laufen klinische Studien zu Immuntherapien und CAR-T-Zell-Therapien. Die Entwicklung von Liquid Biopsys ermöglicht zudem eine präzisere Überwachung ohne invasive Eingriffe.
